Yêu cầu rà soát thuốc gây tê nghi làm 2 sản phụ tử vong
Sau hàng loạt tai biến sản khoa nghiêm trọng xảy ra sau khi gây tê tủy sống giảm đau, Bộ Y tế đã chỉ đạo tăng cường công tác dự phòng phát hiện và xử trí tai biến do gây tê vùng giảm đau trong sản khoa, để đảm bảo cung ứng thuốc tiêm chứa Bupivacaine phục vụ nhu cầu khám, chữa bệnh của người dân.
Ngày 22/11, Cục Quản lý Dược đã gửi công văn hỏa tốc đề nghị Sở tế các tỉnh, thành phố trực thuộc trung ương chỉ đạo cơ sở khám chữa bệnh trên địa bàn; các bệnh viện có giường bệnh trực thuộc Bộ khẩn trương rà soát công tác mua sắm thuốc, đảm bảo cung ứng kịp thời trong trường hợp cần thay thế thuốc đã trúng thầu, chủ động liên hệ với các cơ sở kinh doanh thuốc để được cung ứng.
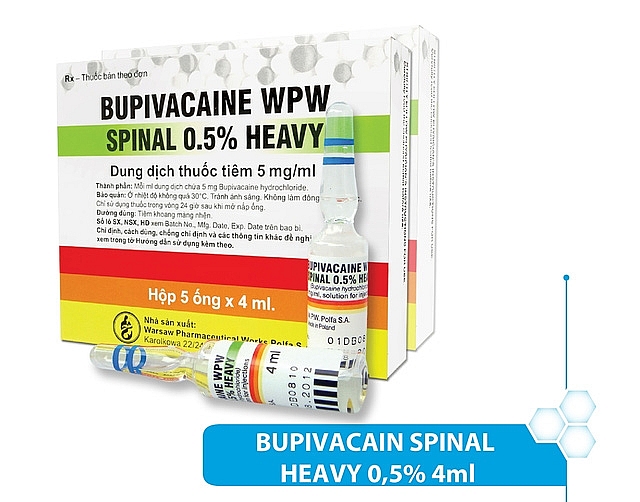 |
| Bộ Y tế yêu cầu rà soát thuốc gây tê có chứa Bupivacaine |
Trong trường hợp không lựa chọn được nhà thầu cung ứng thuốc thông qua hình thức đấu thầu rộng rãi, các cơ sở y tế có thể áp dụng các hình thức lựa chọn nhà thầu phù hợp như mua sắm trực tiếp, chỉ định thầu, chỉ định thầu rút gọn theo quy định luật đấu thầu của Bộ Y tế. Đồng thời, Cục Quản lý Dược cung cấp thông tin về các cơ sở y tế, nhà thầu, thuốc tiêm Bupivacaine trúng thầu năm 2018-2019 và thông tin về cơ sở sản xuất thuốc chứa Bupivacaine đang được lưu hành tại Việt Nam.
Các đơn vị sản xuất, nhập khẩu cũng khẩn trương rà soát tình hình tồn kho, đảm bảo cung ứng thuốc, chủ động tăng cường nguồn cung trong trường hợp có nhu cầu thay thế thuốc.
Trước đó một ngày, Cục Quản lý Dược cũng đã gửi Công văn đến Sở Y tế Cần Thơ phủ nhận những thông tin mà cơ quan này cung cấp cho báo chí liên quan đến thuốc gây tê Bupivacaine WPW Spinal 0,5 Heavy. Công văn do Phó Cục trưởng Cục Quản lý Dược Nguyễn Tấn Đạt ký nêu rõ, ngày 21/11/2019, trên một số báo điện tử có phản ánh việc lãnh đạo Sở Y tế Cần Thơ cho rằng từ tháng 4/2019 đã có công văn báo cáo Cục Quản lý Dược về việc thay thế thuốc gây tê Bupivacaine WPW Spinal 0,5 Heavy (Ba Lan sản xuất).
Tuy nhiên, qua kiểm tra các văn bản, Cục Quản lý Dược lại cho rằng Cục chưa hề nhận được văn bản nào của Sở Y tế Cần Thơ liên quan đến nội dung này.
Cục Quản lý Dược yêu cầu, trong khi chờ cơ quan chức năng xác định nguyên nhân 2 sản phụ tử vong, 1 sản phụ nguy kịch tại Đà Nẵng nghi do dùng thuốc gây mê tủy sống Bupivacaine WPW Spinal 0,5 Heavy, để tránh gây hiểu lầm cho dư luận, Cục Quản lý Dược đề nghị Giám đốc Sở Y tế Cần Thơ báo cáo lại nội dung mà báo chí đã phỏng vấn.
Nguyễn Bách
-

Bộ Y tế cảnh báo nguy cơ từ virus Nipah, Việt Nam siết chặt phòng dịch
-

Chăm sóc sức khỏe nhân dân toàn diện, từ sớm, từ xa và ngay từ cơ sở
-

Bộ Y tế đề nghị gỡ quảng cáo mỹ phẩm vi phạm trên nền tảng mạng xã hội
-

Bộ Y tế thu hồi loạt giấy công bố thực phẩm bảo vệ sức khỏe
-

Cơ cấu tổ chức của Bộ Y tế từ 1/3/2025
- Tử vi tuần mới (4-10/5/2026): Tuổi Mùi tài lộc hanh thông, tuổi Mão thuận buồm xuôi gió
- Tử vi tuần mới (27/4-3/5/2026): Tuổi Tý khẳng định tài năng, tuổi Ngọ sự nghiệp tiến triển
- Đối diện với sự phản bội: "Nếu rẽ trái không được, hãy rẽ phải"
- Tử vi tuần mới (20-26/4/2026): Tuổi Dậu công danh khởi phát, tuổi Mùi xây dựng nền tảng
- Tử vi tuần mới (13-19/4/2026): Tuổi Tuất bản lĩnh phi thường, tuổi Dậu tài lộc vượng phát
- Tử vi tuần mới (6-12/4/2026): Tuổi Hợi sự nghiệp tỏa sáng, tuổi Dần tình duyên nở rộ
- Khơi dậy sự sẻ chia, mở lối hòa nhập cho người tự kỷ
- Tử vi tuần mới (30/3-5/4/2026): Tuổi Mão năng lực vượt trội, tuổi Thìn phần thưởng bất ngờ
























